Reproduktionsmedizin heute: Was eine neue Implantationsstudie wirklich zeigt
30.12.2025
Dr. Maximilian Murtinger
Eine kürzlich in Cell publizierte Arbeit zur menschlichen Embryoimplantation hat in der Fachwelt große Aufmerksamkeit erzeugt. Nicht, weil sie eine neue IVF-Technik vorstellt, sondern weil sie einen biologischen Engpass sichtbar macht, der in der klinischen Praxis seit Jahren bekannt ist – bislang jedoch kaum direkt untersucht werden konnte.
Die Studie zeigt unter kontrollierten Bedingungen, dass erfolgreiche Implantation nicht primär vom Embryo abhängt, sondern von der funktionellen Qualität des Endometriums. Diese Erkenntnis zwingt zu einer nüchternen Neubewertung dessen, wo moderner reproduktionsmedizinischer Fortschritt tatsächlich stattfindet.
Was die Studie wirklich zeigt – eine klinische Lesart
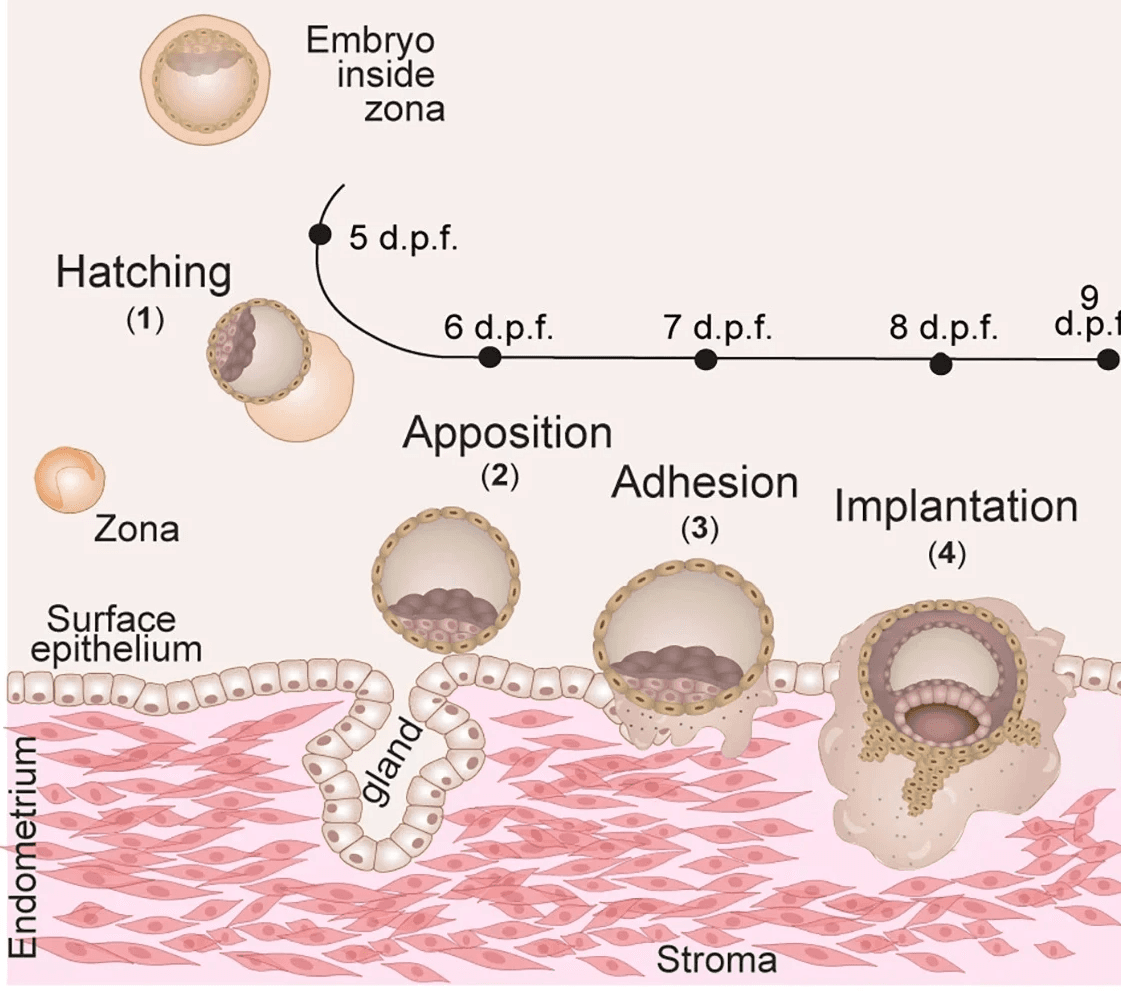
Die Autoren etablieren erstmals ein dreidimensionales, hormonell differenziertes Modell des rezeptiven menschlichen Endometriums, in das humane Embryonen implantieren können. Entscheidend ist dabei nicht die technische Raffinesse des Modells, sondern das Ergebnis.
Implantation gelingt nur dann, wenn das Endometrium funktionell vorbereitet ist – hormonell, stromal, sekretorisch und signalbiologisch. Der Embryo allein, selbst bei morphologischer und genetischer Unauffälligkeit, ist nicht ausreichend.
Die Arbeit macht deutlich:
Implantation ist kein singulärer Moment, sondern ein mehrtägiger biologischer Prozess.
Das Endometrium ist kein passiver Boden, sondern ein aktives, instruktives Organ.
Frühe Plazentationsprozesse sind direkt vom endometrialen Milieu abhängig.
Damit wird experimentell bestätigt, was sich klinisch seit Jahren zeigt: Wiederholtes Implantationsversagen ist häufig kein Embryoproblem, sondern Ausdruck einer gestörten biologischen Antwort des Endometriums.
Die IVF hat ihre technische Reife erreicht.
Der Fortschritt der Reproduktionsmedizin liegt heute in der Biologie – nicht im Labor.
Was sich in der IVF verändert hat – und was nicht
Die letzten Jahre haben die IVF zweifellos verfeinert.
Kulturbedingungen wurden optimiert.
Embryoselektion wird zunehmend durch KI unterstützt.
Genetische Embryoanalysen sind präziser geworden.
All diese Entwicklungen erhöhen Effizienz und Sicherheit. Sie verbessern jedoch nicht die biologische Voraussetzung für Implantation. Sie helfen, Embryonen besser zu beurteilen – nicht, Implantationsfähigkeit herzustellen.
Auch genetische Analysen liefern vor allem eines: Erklärungen. Sie machen Ursachen sichtbar, ersetzen aber keine biologische Vorbereitung.
Was diese Studie bewusst nicht zeigt
So wichtig die Arbeit ist, so klar müssen ihre Grenzen benannt werden.
Sie liefert keinen klinischen Routinetest.
Sie bietet keine therapeutische Anleitung.
Sie bildet die Implantationsrealität nicht vollständig ab.
Immunologische Faktoren, Gefäßentwicklung, systemische Endokrinologie und langfristige Zyklusdynamik sind nicht Teil des Modells. Die Realität ist komplexer, nicht einfacher.
Gerade darin liegt jedoch die eigentliche Aussagekraft der Studie: Implantationsfähigkeit lässt sich nicht technisch erzwingen. Sie entsteht über Zeit – als Ergebnis biologischer Prozesse.
Die klinische Konsequenz
Diese Arbeit verändert nicht die IVF.
Sie verändert den Blick darauf, wann Reproduktionsmedizin beginnt.
Implantation ist kein Ereignis beim Embryotransfer, sondern das Resultat eines lange vorbereiteten biologischen Zustands. Dieser Zustand entsteht vor jeder technischen Maßnahme – über hormonelle Regulation, endometriale Reifung, genetische Voraussetzungen beider Partner und funktionelle Gewebeantwort.
IVF bleibt ein unverzichtbares Werkzeug.
Sie ist jedoch nicht der Ursprung des Problems – und meist auch nicht dessen Lösung.
Einordnung zum Schluss
Der Wert dieser Studie liegt nicht in einer neuen Methode, sondern in einer neuen Klarheit. Sie zwingt dazu, Reproduktionsmedizin wieder dort zu verorten, wo Schwangerschaft biologisch beginnt – lange vor Labor, Technik und Transfer.